|
初中化学 > 木炭还原氧化铜
木炭还原氧化铜
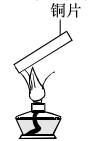
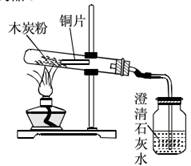
实验步骤 1. 按从下到上安装好仪器,试管中略向下倾斜。 2. 将木炭粉和黑色氧化铜分别充分烘干后,按一定的质量比称取两种黑色粉末。放入研钵中反复研碎、混匀。 3. 用药匙或小纸槽将黑色混合物放进试管底部,塞上带有橡皮塞的直角玻璃导管,玻璃导管的另一端插入另一支盛有澄清石灰水的试管中。 4. 点燃酒精灯,先预热试管,然后集中在盛有混合粉末处加强热。 5. 几分钟后,可观察到澄清石灰水变混浊。 6. 拔下橡皮塞,熄灭酒精灯,待试管自然冷却后,将试管中的混合物倒到一张白纸上。 7. 混合粉末中有红色的单质铜生成。 反应原理 说明 1. 酒精喷灯产生的温度较高,因此,盛有混合粉末的试管应选用耐高温的硬质试管,用一般的试管会烧红穿孔。 2. 如条件允许,可用管道煤气灯来加热。 3. 所选用的木炭粉和氧化铜粉末一定要烘干,否则实验现象不明显。 木炭可以还原氧化铜生成红色铜单质和二氧化碳气体。 1. 反应方程式 2. 反应基本类型 3. 实验现象 木炭还原氧化铜的实验中正确的是( ) A. 装药品时先装氧化铜,再装木炭粉 B. 由于没有液体生成,试管口可以略向上倾斜 C. 实验结束后等试管冷却再把导气管拿走 D. 生成的气体不能使石灰水变浑浊 试题难度:中 分析:反应物都为固体,要充分混合均匀再装入试管;只要是加热固体就要使试管口略向下倾斜,防药品潮湿产生水分倒流;实验结束后如果试管没有冷却就让生成物接触空气,会使生成的铜再被氧化。 答案:C 木炭还原氧化铜实验的改进 木炭还原氧化铜在初中阶段是一个很重要的实验。所以本次实验的成功与否至关重要。 1、原实验 在教材中该实验是采用经烘干的木炭粉末和氧化铜粉末共同加热来进行的。但我们在实际操作中发现采用氧化铜粉末进行实验对实验效果有很大的影响。具体影响如下:氧化铜粉末从黑色变成红色这一实验现象在实际操作中往往难以观察;木炭的颜色是黑色,还原后的铜的颜色是红色,本来是很容易分辨的。但是,使用氧化铜粉末与木炭粉混合物作为药品,当木炭粉或氧化铜粉末过量时,实验后铜粉的红色都会被黑色所覆盖,很难观察到铜粉的颜色。实验操作步骤在实际中难以完成;使用氧化铜粉末,必须等混合物完全冷却后从试管中倒出。虽然木炭粉末经过烘干,但是因为木炭特别是粉末具有较强的吸附能力,在实验后还是无可避免的在试管中凝聚了一些水,这给转移混合物造成了一定的困难。 2、改进后的实验 针对原实验的以上不足,可以尝试把原实验中的氧化铜粉末改成表面覆盖有一层氧化铜的铜片进行实验。发现实验现象非常明显,而且操作简便,还能达到对比实验现象的效果。具体操作步骤如下: 取一片长约7-8cm,宽约1cm的铜片,把表面可能存在的氧化物用砂纸除去。 在酒精灯上加热,使之表面生成一层氧化铜,如下图所示。或把铜片烧红后立即伸入集满氧气的集气瓶中,经过这样处理的铜片表面的氧化铜更均匀,实验的效果更明显。为了达到对比的效果,不要把整片铜片都镀上氧化铜,但在平时的课堂操作中,在空气中处理也可以达到不错的实验效果。 在一干燥的试管中装入不超试管容积1/3 观察到澄清石灰水变浑浊后,移走导管,停止加热。待试管逐渐冷却后,用镊子把铜片夹出。洗净铜片表面的木炭粉,观察现象。 3、注意事项 给铜片镀上的氧化铜最好是新制的,笔者发现使用隔天镀上的氧化铜的效果不是很理想。最好在上课前十分钟处理好铜片。 4、体会 使用覆盖有氧化铜的铜片代替氧化铜粉末具有操作简便、现象明显、便于观察现象的特点,而且实验后的铜片可以循环使用,在很大的程度上节约了药品。  北京高拓电子科技有限责任公司 北京壹灵壹教育科技股份有限公司 Copyright 2015-2016 chinaedu.com,All Rights Reserved 京ICP备11011674号-1 全国客服电话:400-6869-101 传真:010-84640631  |




















分析一下影响木炭还原氧化铜实验的因素有哪些?