|
初中化学 > 氢氧化钠与三氯化铁反应
氢氧化钠与三氯化铁反应
实验步骤 1. 试管中滴加棕黄色的三氯化铁溶液2毫升。 2. 再向试管中滴加1毫升氢氧化钠溶液,随即产生红褐色的氢氧化铁沉淀。 实验原理 FeCl3 + 3NaOH ==Fe(OH)3↓+ 3NaCl 氢氧化钠跟氯化铁溶液反应生成红褐色沉淀氢氧化铁和氯化钠。
1. 化学方程式 2. 实验现象 3. 相关拓展知识 1. 某同学想用实验证明FeCl3溶液的黄色不是由Cl-造成的,下列实验无意义的是( )
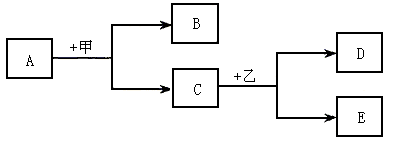
A. 方案②、方案③ B. 方案③、方案④ C. 方案④ D. 方案① 试题难度:中 2. 下图是初中化学常见的物质之间相互转化关系的示意图。其中A是一种难溶于水的金属氧化物,乙是一种碱溶液。请回答下列问题: (1)如果D是一种蓝色沉淀,则A为_____________,写出A跟甲反应的化学方程式____________________________________________________。 (2)如果C是一种黄色溶液的溶质,则A为_____________,写出C跟乙反应的化学方程式____________________________________________________。 试题难度:难 1 分析:证明FeCl3溶液的黄色不是由Cl-造成的,就要抓住Fe3+和Cl-。方案①说明不显黄色;方案②说明Fe3+被沉淀后,溶液不显黄色;方案③说明Cl-被沉淀后溶液仍显黄色。方案④只说明溶液稀释颜色变浅。 答案:D 2 分析:这是一道元素化合物推断题。要求我们熟练掌握各反应的典型特征,从而找到入手点。尤其是熟练记忆实验现象,帮助我们来做好这类题目。注意找到入手点后前后都要依次推出,即使不是所要求的问题,这样可以验证我们的推断是否正确。D是一种蓝色沉淀,则就是氢氧化铜,往回推出相关物质并不难了。C是一种黄色溶液的溶质,说明C中含有Fe3+。 制备氢氧化铁胶体 把适量三氯化铁溶液滴入沸水中即得氢氧化铁胶体。在沸水中制备是因为Fe3+水解倾向因温度升高而增强(FeCl3+3H2O 因氢氧化铁胶体受热聚沉为Fe(OH)3,所以对沉淀进行实验。混合FeCl3溶液和NaOH溶液得沉淀,均分成2份。往第1份中加HCl,边加边搅拌,直到沉淀恰好完全溶解为止,记下所加HCl的滴数(设为20滴);对第2份小心加热至沸并维持一段时间,冷却到室温,Fe(OH)3沉淀的颜色变深了。如上加HCl直到Fe(OH)3沉淀恰好完全溶解为止,所加HCl的滴数必超过20滴,超过多少滴和维持加热时间成正比。表明受热后,Fe(OH)3(相对于未受热而言)较难溶于酸,所以,经受热形成的胶体在冷却后并不溶解或难溶解。 事实上,氢氧化铁化学式是Fe2O3·xH2O,制得的沉淀在放置或(和)加热过程中。x值下降,表现为沉淀颜色变深,(相对)难溶于酸。这是许多高价金属氢氧化物,如Al2O3·xH2O、Cr2O3·xH2O的通性,只是Al2O3·xH2O的白颜色不可能改变。  北京高拓电子科技有限责任公司 北京壹灵壹教育科技股份有限公司 Copyright 2015-2016 chinaedu.com,All Rights Reserved 京ICP备11011674号-1 全国客服电话:400-6869-101 传真:010-84640631  |




















取少量氢氧化钠溶液滴入氯化亚铁溶液中,观察现象及静置后发生的变化,讨论原因。